Dịch vụ công bố tiêu chuẩn Hóa chất QC dùng cho Hệ thống máy phân tích dòng chảy tế bào của BD
Ngày 12/09/2024 - 10:09Trang thiết bị y tế công bố tiêu chuẩn áp dụng:
- Tên trang thiết bị y tế: Hóa chất QC dùng cho Hệ thống máy phân tích dòng chảy tế bào của BD
- Tên thương mại (nếu có):
- Mã Global Medical Device Nomenclature - GMDN (nếu có):
- Chủng loại:
- Mã sản phẩm:
- Quy cách đóng gói (nếu có):
- Loại trang thiết bị y tế: TTBYT Loại A
- Mục đích sử dụng:
- Tên cơ sở sản xuất:
- Địa chỉ cơ sở sản xuất:
- Nước cơ sở sản xuất:
- Tiêu chuẩn chất lượng sản phẩm áp dụng: ISO 13485: 2003 & EN ISO 13485: 2012
Đối với trang thiết bị y tế chứa chất ma túy, tiền chất (nếu có):
Thông tin về chủ sở hữu trang thiết bị y tế:
Thông tin về cơ sở bảo hành:
Số công bố đủ điều kiện sản xuất đối với trang thiết bị y tế sản xuất trong nước:

Giới thiệu về Hóa chất QC
Hóa chất QC (Quality Control) là các dung dịch và vật liệu được sử dụng để kiểm tra và hiệu chuẩn hệ thống máy phân tích dòng chảy tế bào, đảm bảo rằng thiết bị hoạt động chính xác và cung cấp kết quả đáng tin cậy. Đối với các hệ thống máy phân tích dòng chảy tế bào của BD (Becton, Dickinson and Company), việc sử dụng hóa chất QC đúng cách là rất quan trọng để duy trì hiệu suất và chất lượng của các phân tích tế bào.
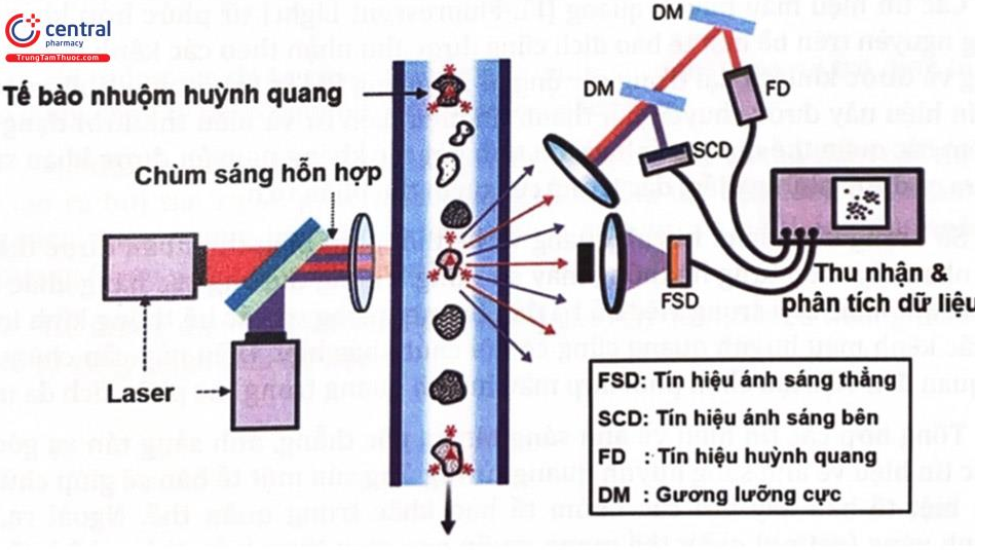
Các Loại Hóa chất QC Thường Dùng
+ Hóa chất QC Tế Bào (Cell QC Reagents):
Tế bào chuẩn (Calibration Beads): Dùng để hiệu chỉnh và kiểm tra độ chính xác của hệ thống phân tích. Các hạt này có kích thước, màu sắc và độ phát quang đã được xác định rõ ràng để đảm bảo rằng hệ thống máy phân tích đo lường chính xác các tham số tế bào.
Tế bào điều khiển (Control Cells): Các tế bào với các đặc điểm cụ thể, như phân bố kích thước và nội dung tế bào, dùng để kiểm tra khả năng phân tích của thiết bị và xác minh rằng kết quả thu được nằm trong giới hạn kiểm tra quy định.
+ Dung dịch Chuẩn (Standard Solutions):
Dung dịch chuẩn phân tích (Analytical Standards): Dùng để tạo ra các điểm chuẩn cho việc phân tích các thông số tế bào như kích thước, độ phức tạp, và mức độ phát quang. Các dung dịch này giúp đảm bảo độ chính xác và độ tin cậy của các phép đo.
+ Hóa chất QC Phân Tích (Assay QC Reagents):
Dung dịch kiểm tra tính năng (Performance Testing Solutions): Dùng để đánh giá hiệu suất của máy phân tích trong các bài kiểm tra cụ thể, như kiểm tra độ nhạy và độ đặc hiệu của hệ thống.
+ Dung dịch Khử Trùng và Làm Sạch (Cleaning and Disinfecting Solutions):
Dung dịch khử trùng (Disinfectants): Được sử dụng để làm sạch các phần của hệ thống máy phân tích nhằm tránh nhiễm bẩn và đảm bảo môi trường phân tích không bị ô nhiễm.
Quy trình Sử dụng Hóa chất QC
+ Chuẩn bị và Lưu trữ:
Đảm bảo hóa chất QC được bảo quản ở điều kiện nhiệt độ và ánh sáng phù hợp theo hướng dẫn của nhà sản xuất. Đọc kỹ hướng dẫn sử dụng để chuẩn bị hóa chất trước khi kiểm tra hoặc hiệu chỉnh thiết bị.
+ Sử dụng và Kiểm tra:
Hiệu chỉnh: Sử dụng các dung dịch chuẩn và tế bào QC để thực hiện các bước hiệu chỉnh thiết bị, đảm bảo rằng máy phân tích dòng chảy tế bào đo lường chính xác các tham số của mẫu.
Kiểm tra: Thực hiện các bài kiểm tra chất lượng theo quy trình quy định để xác nhận rằng thiết bị hoạt động đúng cách và kết quả phân tích đáp ứng các tiêu chuẩn chất lượng.
+ Ghi Chép và Báo cáo:
Ghi lại các kết quả kiểm tra chất lượng và hiệu chỉnh trong nhật ký bảo trì thiết bị. Đảm bảo rằng mọi bất thường hoặc kết quả không đạt yêu cầu được báo cáo và xử lý kịp thời.
Quy định và Công bố Sản phẩm tại Việt Nam
Trước khi hóa chất QC dùng cho hệ thống máy phân tích dòng chảy tế bào được đưa vào lưu hành tại thị trường Việt Nam, doanh nghiệp cần thực hiện quy trình công bố sản phẩm theo quy định của Bộ Y tế Việt Nam. Quy trình này nhằm đảm bảo rằng sản phẩm đáp ứng đầy đủ các yêu cầu về chất lượng và an toàn.
+ Quy trình Công bố Sản phẩm:
Chuẩn bị Hồ sơ: Doanh nghiệp cần chuẩn bị hồ sơ bao gồm thông tin về sản phẩm, chứng nhận chất lượng, hướng dẫn sử dụng, và các tài liệu liên quan khác. Hồ sơ cần được dịch sang tiếng Việt và có chứng thực hợp lệ.
Nộp Hồ sơ cho Cục Quản lý Dược: Hồ sơ công bố sẽ được gửi tới Cục Quản lý Dược thuộc Bộ Y tế để tiến hành đánh giá và thẩm định.
Đánh giá và Thẩm định: Cục Quản lý Dược sẽ tiến hành đánh giá các tài liệu và thông tin về sản phẩm. Có thể yêu cầu kiểm tra thực tế sản phẩm tại cơ sở sản xuất hoặc nhập khẩu.
Cấp Giấy chứng nhận Công bố: Sau khi hoàn tất đánh giá, nếu sản phẩm đáp ứng các yêu cầu, Cục Quản lý Dược sẽ cấp Giấy chứng nhận công bố sản phẩm, cho phép sản phẩm được lưu hành tại Việt Nam.
+ Các yêu cầu quan trọng:
Chứng nhận chất lượng: Sản phẩm cần có chứng nhận chất lượng từ cơ quan có thẩm quyền, như chứng nhận ISO hoặc các chứng nhận tương đương.
Hồ sơ Kỹ thuật: Hồ sơ công bố phải bao gồm các tài liệu kỹ thuật chi tiết về sản phẩm, hướng dẫn sử dụng và thông tin bảo quản.
Tuân thủ Quy chuẩn Việt Nam: Sản phẩm phải tuân thủ các quy chuẩn và quy định của Việt Nam về hóa chất và thiết bị y tế.
Kết luận
Hóa chất QC là yếu tố quan trọng trong việc duy trì hiệu suất và độ chính xác của hệ thống máy phân tích dòng chảy tế bào. Việc sử dụng và quản lý hóa chất QC đúng cách giúp đảm bảo kết quả xét nghiệm đáng tin cậy và bảo trì thiết bị ở trạng thái hoạt động tốt nhất. Quy trình công bố sản phẩm tại Việt Nam là bước cần thiết để đảm bảo rằng sản phẩm đáp ứng các yêu cầu chất lượng và an toàn trước khi được đưa vào lưu hành.










