Chứng nhận Nhóm Trang thiết bị y tế theo tiêu chuẩn Quốc gia TCVN 6591-4:2021
Ngày 28/08/2024 - 01:08Lời nói đầu
TCVN 6591-4:2021 thay thế TCVN 6591-4:2008;
TCVN 6591-4:2021 hoàn toàn tương đương với ISO 8536-4:2019;
TCVN 6591-4:2021 do Viện Trang thiết bị và Công trình y tế biên soạn, Bộ Y tế đề nghị, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
Bộ tiêu chuẩn TCVN 6591 (ISO 8536) Thiết bị truyền dịch dùng trong y tế, gồm các phần sau:
TCVN 6591-1:2021 (ISO 8536-1:2011) Phần 1: Chai thủy tinh chứa dịch truyền
TCVN 6591-2:2021 (ISO 8536-2:2010) Phần 2: Nút chai chứa dịch truyền
TCVN 6591-3:2021 (ISO 8536-3:2009) Phần 3: Nắp nhôm dùng cho chai chứa dịch truyền
TCVN 6591-4:2021 (ISO 8536-4:2019) Phần 4: Bộ dây truyền dịch dùng một lần dẫn truyền bằng trọng lực
TCVN 6591-5:2019 (ISO 8536-5:2004) Phần 5: Bộ buret truyền dịch dùng một lần, dẫn truyền bằng trọng lực
Bộ tiêu chuẩn ISO 8536 Infusion equipment for medical use, gồm các phần sau:
Part 6: Freeze drying closures for infusion bottles
Part 7: Caps made of aluminium-plastics combinations for infusion bottles
Part 8: Infusion equipment for use with pressure infusion apparatus
Part 9: Fluid lines for use with pressure infusion equipment
Part 10: Accessones for fluid lines for use with pressure infusion equipment
Part 11: Infusion filters for use with pressure infusion equipment
Part 12: Check valves
THIẾT BỊ TRUYỀN DỊCH DÙNG TRONG Y TẾ - PHẦN 4: BỘ TRUYỀN DỊCH DÙNG MỘT LẦN DẪN TRUYỀN BẰNG TRỌNG LỰC
Phạm vi áp dụng
Tiêu chuẩn này quy định các yêu cầu cho bộ truyền dịch sử dụng một lần, hoạt động nhờ trọng lực dùng trong y tế nhằm mục đích đảm bảo sự tương thích của chúng với các chai chứa dịch truyền và thiết bị truyền tĩnh mạch.
Mục đích thứ hai của tiêu chuẩn này là cung cấp chỉ dẫn về các đặc tính liên quan đến chất lượng và tính năng của các vật liệu sử dụng trong các bộ truyền dịch và để trình bày các ký hiệu dùng cho các thành phần của bộ truyền dịch.
Tài liệu viện dẫn
Các tài liệu viện dẫn sau rất cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
TCVN 4851 (ISO 3696), Nước dùng để phân tích trong phòng thí nghiệm.
TCVN 6916-1 (ISO 15223-1), Trang thiết bị y tế - Ký hiệu sử dụng với nhãn trang thiết bị y tế, ghi nhãn và cung cấp thông tin - Phần 1: Yêu cầu chung.
TCVN 8664-1 (ISO 14644-1), Phòng sạch và môi trường kiểm soát liên quan - Phần 1: Phân loại độ sạch không khí.
ISO 7864, Sterile hypodermic neddles for single use (Kim tiêm dưới da vô khuẩn sử dụng một lần).
ISO 8536-13, Infusion equipment for medical use - Part 13: Graduated flow regulators for single use with fluid contact (Thiết bị truyền dịch dùng trong y tế - Phần 13: Bộ điều tiết dòng chảy chia độ sử dụng một lần khi tiếp xúc với chất lỏng)
ISO 8536-14, Infusion equipment for medical use - Part 14: Clamps and flow regulators for transfusion and infusion equipment without fluid contact (Thiết bị truyền dịch dùng trong y tế - Phần 14: Kẹp và bộ điều tiết dòng chảy để truyền và thiết bị truyền dịch không tiếp xúc với chất lỏng)
ISO 80369-7, Small-bore connectors for liquids and gases in healthcare applications -Part 7: Connectors for intravascular or hypodermic applications (Đầu nối nòng nhỏ cho chất lỏng và khí trong các ứng dụng chăm sóc sức khỏe - Phần 7: Đầu nối cho các ứng dụng nội mạch hoặc dưới da)
Thuật ngữ và định nghĩa
Không có thuật ngữ và định nghĩa được đưa ra trong tiêu chuẩn này.
Yêu cầu chung
+ Thuật ngữ sử dụng cho các thành phần của các bộ truyền dịch và của một thiết bị dẫn khí riêng biệt quy định trong Hình 1, 2 và 3. Những hình này minh họa các ví dụ về cấu hình các bộ truyền dịch và các thiết bị dẫn khí; có thể sử dụng các cấu hình khác miễn là chúng đem lại kết quả tương tự. Các bộ truyền dịch quy định trong Hình 2 chỉ nên sử dụng cho các túi đựng bằng chất dẻo có thể xẹp. Các bộ truyền dịch quy định trong Hình 2 sử dụng với các thiết bị dẫn khí-riêng biệt quy định trong Hình 3, hay các bộ truyền dịch quy định trong Hình 1 cần sử dụng cho các chai đựng cứng.
+ Bộ truyền dịch cần được cung cấp các chụp bảo vệ. Thiết bị dẫn khí cần được cung cấp một chụp bảo vệ trên kim hay thiết bị đâm xuyên nắp đậy lọ truyền dịch (xem Hình 3).
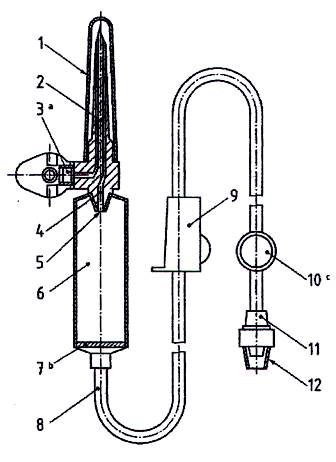
CHÚ DẪN:
1) Nắp bảo vệ của thiết bị đâm xuyên 2) Thiết bị đâm xuyên nắp chai 3) Đường dẫn khí vào với màng lọc và nắp đậy 4) Kênh dẫn dịch 5) Ống nhỏ giọt 6) Buồng nhỏ giọt | 7) Bộ lọc dịch 8) Ống dẫn 9) Điều tiết dòng chảy 10) Vị trí bơm thuốc 11) Đầu côn đực 12) Chụp bảo vệ đầu nối đực |
a nắp đậy của thiết bị dẫn khí là tùy chọn
b Bộ lọc dịch có thể đặt ở những chỗ khác, tốt hơn là gần cửa vào bệnh nhân,.
c Vị trí bơm là tùy chọn
Hình 1-Ví dụ về một bộ truyền dịch có thông khí
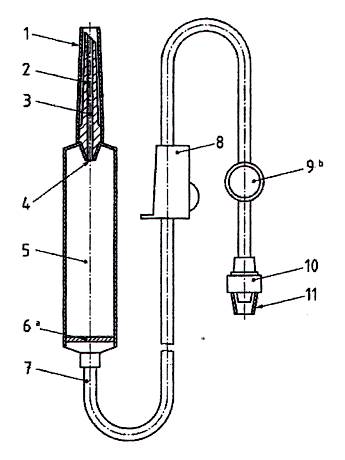
CHÚ DẪN:
1) Nắp bảo vệ của thiết bị đâm xuyên 2) Thiết bị đâm xuyên nắp chai 3) Kênh dẫn dịch 4) Ống nhỏ giọt 5) Buồng nhỏ giọt 6) Bộ lọc dịch | 7) Bộ lọc dịch 8) Ống dẫn 9) Vị trí bơm thuốc 10) Đầu côn đực 11) Chụp bảo vệ đầu nối đực |
a Bộ lọc dịch có thể đặt ở những chỗ khác, tốt hơn là gần cửa vào bệnh nhân.
b Vị trí bơm là tùy chọn
Hình 2 - Ví dụ về một bộ truyền dịch không thông khí
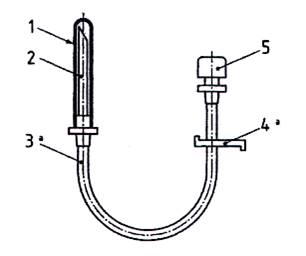
CHÚ DẪN:
1) Chụp bảo vệ 2) Thiết bị hoặc kim xuyên qua nắp đậy 3) Đường ống | 4) Kẹp giữ 5) Lối vào khí có màng lọc |
a Các thiết kế khác có thể chấp nhận được nếu đảm bảo các khía cạnh an toàn tương tự
Hình 3 - Ví dụ về một thiết bị dẫn không khí vào
Ký hiệu
Ký hiệu phải tuân theo các yêu cầu về ghi nhãn theo Điều 10.
Vật liệu
Vật liệu sản xuất bộ truyền dịch, các thành phần của nó và thiết bị dẫn khí vào độc lập (quy định trong Điều 4) phải phù hợp với các yêu cầu quy định trong Điều 7. Trong trường hợp các thành phần của bộ truyền dịch đến tiếp xúc trực tiếp với dịch truyền, các vật liệu cũng phải phù hợp với các yêu cầu quy định trong Điều 8 và 9.
Yêu cầu vật lý
+ Nhiễm thể hạt
Các bộ truyền dịch phải được sân xuất trong các điều kiện tối thiểu hóa sự nhiễm hạt. Tất cả các phần cần phải nhẵn và sạch tại các bề mặt dẫn dịch. Khi thử nghiệm như quy định trong A.2, số lượng hạt phải không vượt quá giới hạn chỉ số nhiễm.
+ Rò rỉ
Bộ truyền dịch khi thử nghiệm theo A.3 phải không có dấu hiệu rò khí.
+ Độ bền kéo giãn
Khi thử nghiệm như đã nêu rõ trong A.4, bộ truyền dịch, ngoại trừ chụp bảo vệ, phải chịu được lực kéo tĩnh không dưới 15 N trong vòng 15 min.
+ Thiết bị đâm xuyên nắp đậy
Kích thước của thiết bị xuyên nắp đậy phải phù hợp với các kích thước thể hiện trong Hình 4. Mặt cắt ngang của thiết bị xuyên nắp trên độ dài 15 mm phải là một hình tròn.
CHÚ THÍCH: Kích thước 15 mm trong Hình 4 là số đo tham chiếu.
Thiết bị xuyên nắp cần có khả năng đâm và xuyên qua nắp đậy của một chai truyền dịch không đâm thủng trước. Trong thao tác này không nên tạo mành lõi.
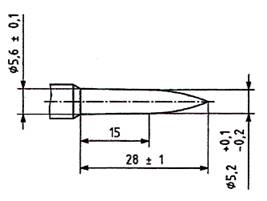
Hình 4 - Kích thước của thiết bị đâm xuyên nắp đậy
+ Thiết bị dẫn khí vào
Thiết bị dẫn khí vào có thể là một phần không thể thiếu của bộ truyền dịch (Hình 1) hoặc một thiết bị độc lập (Hình 3).
Thiết bị dẫn khí vào phải được cung cấp một màng lọc khí để phòng ngừa sự xâm nhập vi sinh vật vào trong chỗ mà thiết bị được cài vào.
Khi thiết bị dẫn khí vào được sử dụng, không khí được đưa vào chai phải không được cuốn theo đường vào của chất lỏng của thiết bị đâm xuyên.
Màng lọc khí và thiết kế của thiết bị dẫn khí vào phải sao cho tất cả không khí đi vào chai chứa cứng đều đi qua nó và làm sao để dòng dịch không bị giảm quá 20 % so với dòng dịch từ chai chứa thông khí tự do khi thử nghiệm theo A.5.2 và A.5.3.
Thiết bị xuyên nắp cần có khả năng đâm và xuyên qua nắp đậy của một chai truyền dịch không đâm thủng trước. Trong thao tác này không nên tạo mảnh lõi.
+ Ống dẫn
Ống dẫn làm từ vật liệu mềm, cần trong hoặc đủ trong để có thể quan sát được giao diện không khí và nước trong quá trình bọt khí đi qua bằng mắt thường.
Ống dẫn từ đầu dưới của buồng nhỏ giọt không được dài quá 1 500 mm, kể cả vị trí bơm (nếu có) và đầu nối côn đực.
+ Bộ lọc dịch
Bộ truyền dịch cần được cung cấp một bộ lọc dịch.
Khi thử nghiệm theo A.6, khả năng giữ các thể hạt cao su trên màng lọc không được dưới 80 %.
+ Buồng nhỏ giọt và ống nhỏ giọt
Buồng nhỏ giọt phải cho phép quan sát liên tục sự rơi của các giọt dịch. Dịch đi vào buồng nhỏ giọt qua một ống nhô vào trong buồng. Cần có khoảng cách không dưới 40 mm giữa đầu cuối của ống nhỏ giọt và đầu ra của buồng nhỏ giọt, hay khoảng cách không dưới 20 mm giữa ống nhỏ giọt và bộ lọc dịch. Thành của buồng nhỏ giọt phải không gần hơn 5 mm với đầu cuối của ống nhỏ giọt, ống nhỏ giọt phải làm sao để 20 giọt nước cất hoặc 60 giọt nước cất ở nhiệt độ (23 ± 2) °C với lưu lượng (50 ± 10) giọt/min sẽ cung cấp một thể tích (1 ± 0,1) ml hay khối lượng (1 ± 0,1) g. Buồng nhỏ giọt nên cho phép và tạo dễ dàng cho thao tác mồi.
+ Điều tiết dòng chảy
Điều tiết dòng chày phải phù hợp với ISO 8536-13 hoặc ISO 8536-14.
+ Lưu lượng dòng của bộ truyền dịch
Bộ truyền dịch không sử dụng thiết bị dẫn khí vào phải cung cấp không dưới 1000 ml dung dịch NaCl (nồng độ NaCl = 9 g/l) trong vòng 10 min cho một ống nhỏ giọt cung cấp 1 ml với 20 giọt. Thử nghiệm phải phù hợp với A.5.1.
+ Vị trí bơm thuốc
Khi được cung cấp, vị trí bơm tự kín phải kín lại khi thử nghiệm theo A.7 và cần phải không bị rò rỉ nước. Vị trí bơm nên để gần đầu nối côn đực.
+ Đầu nối côn đực
Đầu cuối của đường ống phải kết thúc ở một đầu nối côn đực phù hợp với ISO 80369-7.
+ Chụp bảo vệ
Các chụp bảo vệ phải bao phủ các bề mặt tương ứng của thiết bị truyền dịch để ngăn ngừa ô nhiễm từ môi trường xung quanh, tránh chấn thương do dính và hư hỏng bao bì. Các chụp bảo vệ nên chắc chắn nhưng dễ dàng tháo bỏ.
Yêu cầu hóa học
+ Chất khử (có thể bị ô xi hóa)
Khi thử nghiệm theo B.2, sự khác biệt thể tích của dung dịch Na2S2O3 [nồng độ Na2S2O3 = 0,005 mol/l] làm dung dịch chiết S1 và của thể tích Na2S2O3 làm dung dịch rỗng S0 phải không quá 2,0 ml.
+ Ion kim loại
Dung dịch chiết không được chứa quá 1 μg/ml các ion bari, clo, đồng, chì và thiếc và không quá 0,1 μg/ml ion cadimi khi xác định bằng phép đo quang phổ hấp thu nguyên tử (AAS) hoặc một phương pháp tương đương.
Khi thử nghiệm theo B.3, cường độ màu tạo ra trong dung dịch thử nghiệm không được vượt quá cường độ màu của dung dịch đối chiếu tương ứng có nồng độ khối lượng p(Pb2+) = 1 μg/ml.
+ Chuẩn độ tính axit hoặc tính kiềm
Khi thử nghiệm theo B.4, cần có không quá 1 ml dung dịch thể tích chuẩn axit hoặc kiềm làm chất chỉ thị sự thay đổi màu sang màu xám.
+ Tồn dư khí bay hơi
Khi thử nghiệm theo B.5, tổng lượng tồn dư khô không được vượt quá 5 mg.
+ Sự hấp thu tia cực tím (UV) của dung dịch chiết
Khi thử nghiệm theo B.6, dung dịch chiết S1 phải S(λ) < 0,1 với λ trong phạm vi từ 250 mm đến 320 mm.
Yêu cầu sinh học
+ Yêu cầu chung
Bộ truyền dịch và thiết bị dẫn khí vào độc lập phải được đánh giá tính tương thích sinh học theo các chỉ dẫn nêu trong C.2.
+ Tính vô khuẩn
Bộ truyền dịch và thiết bị dẫn khí vào độc lập, khi ở trong bao bì đơn vị của chúng phải trải qua quá trình tiệt khuẩn đã xác thực, ví dụ TCVN 7392-1 (ISO 11135), TCVN 7393 (ISO 11137) và ISO 17665.
+ Tính gây sốt
Bộ truyền dịch và thiết bị dẫn khí vào độc lập phải được đánh giá không có chất gây sốt bằng cách sử dụng một thử nghiệm thích hợp. Kết quả thử nghiệm phải chứng tỏ rằng bộ truyền dịch và thiết bị dẫn khí vào độc lập không có chất gây sốt. Chỉ dẫn thử nghiệm tính gây sốt được nêu trong C.1.
+ Tan huyết
Bộ truyền dịch phải được đánh giá không chứa các thành phần gây tan huyết Kết quả thử nghiệm phải chứng tỏ rằng bộ truyền dịch không gây ra các phản ứng tan huyết Chỉ dẫn về thử nghiệm tìm các thành phần gây tan huyết được nêu trong ISO 10993-4.
+ Độc tính
Cần đánh giá độc tính của các vật liệu bằng cách tiến hành các thử nghiệm thích hợp, và kết quả thu được cần chứng tỏ chúng không có độc tính. Chỉ dẫn về thử nghiệm độc tính được thể hiện trong TCVN 7391-1 (ISO 10993-1).
Ghi nhãn
+ Yêu cầu chung
Việc ghi nhãn phải bao gồm các yêu cầu như quy định trong 10.2 và 10.3. Nếu các ký hiệu đồ họa được sử dụng, tham khảo TCVN 6916 (ISO 15223-1).
CHÚ THÍCH: Sự hiện diện của các chất cần quan tâm có thể được chỉ ra bằng cách sử dụng ký hiệu 2725 của ISO 7000 bằng cách thay thế “XXX” bằng tên viết tắt của chất đó. Sự vắng mặt của các chất cần quan tâm có thể được chỉ ra bằng cách gạch ngang ký hiệu tương ứng.
+ Bao bì đơn vị
Bao bì đơn vị cần được ghi nhãn với ít nhất thông tin sau:
a) tên và địa chỉ của nhà sản xuất;
b) một mô tả các thành phần bên trong;
c) chỉ báo rằng bộ truyền dịch không chứa chất gây sốt, hoặc chỉ báo rằng bộ truyền dịch không chứa nội độc tố vi khuẩn;
d) ký hiệu đồ họa chỉ báo rằng bộ truyền dịch vô khuẩn như thể hiện trong TCVN 6196-1 (ISO 15223-1);
e) ký hiệu lô (mẻ) bắt đầu bằng chữ “LOT”, hoặc sử dụng một ký hiệu đồ họa phù hợp với TCVN 6196-1 (ISO 15223-1);
f) hạn sử dụng tới tháng và năm, kèm theo một chữ thích hợp hoặc ký hiệu đồ họa phù hợp với TCVN 6196-1 (ISO 15223-1);
g) chỉ báo rằng bộ truyền dịch chỉ sử dụng một lần, hoặc các chữ tương đương, hoặc sử dụng ký hiệu đồ họa phù hợp với TCVN 6196-1 (ISO 15223-1);
h) chữ cái “G”, viết tắt của trọng lực và có chiều cao kiểu chữ sẽ nổi bật rõ ràng so với văn bản xung quanh;
i) một công bố rằng 20 giọt nước cất hay 60 giọt nước cất cung cấp bởi ống nhỏ giọt tương đương với thể tích (1 ± 0,1) ml hoặc khối lượng (1 ± 0,1) g;
j) các kích thước danh nghĩa của kim tiêm tĩnh mạch, nếu có kèm theo.
Nếu không gian có sẵn quá nhỏ để cung cấp tất cả thông tin này bằng các ký tự và / hoặc ký hiệu dễ đọc, thông tin có thể giảm thành e) và f). Trong trường hợp này, thông tin như yêu cầu trong điều này sẽ được ghi trên nhãn của kệ lớn hơn tiếp theo hoặc bao bì nhiều đơn vị.
+ Kệ hoặc bao bì nhiều đơn vị
Kệ hoặc bao bì nhiều đơn vị phải được ghi nhãn với ít nhất thông tin sau:
a) tên và địa chỉ của nhà sản xuất;
b) một mô tả các thành phần bên trong;
c) ký hiệu lô (mẻ), bắt đầu bằng chữ “LOT”, hoặc sử dụng một ký hiệu đồ họa phù hợp với TCVN 6196-1 (ISO 15223-1);
d) Hạn sử dụng theo năm và tháng, kèm theo chữ thích hợp hoặc ký hiệu đồ họa theo TCVN 6196-1 (ISO 15223-1);
e) hướng dẫn sử dụng, bao gồm cả cảnh báo, ví dụ: về các chụp bảo vệ đã tách rời (hướng dẫn sử dụng cũng có thể ở dạng tờ hướng dẫn);
f) chữ cái “G”, viết tắt của trọng lực và có chiều cao kiểu chữ sẽ nổi bật rõ ràng so với văn bản xung quanh;
g) một ghi chú lưu trữ, nếu có.
Bao gói
+ Bộ truyền dịch và thiết bị dẫn khí phải được bao gói riêng biệt làm sao để chúng vẫn còn vô khuẩn trong thời gian bảo quản. Bao bì đơn vị cần phải đóng kín theo kiểu dễ phát hiện bằng chứng can thiệp.
+ Bộ truyền dịch và thiết bị dẫn khí phải được đóng gói và tiệt khuẩn theo cách không xuất hiện các vùng bị bẹp hoặc xoắn lại làm hạn chế tính năng của bộ truyền dịch khi chúng chuẩn bị sử dụng.
Loại bỏ
Cần cung cấp thông tin để xử lý an toàn và hợp lý với môi trường đối với các bộ truyền dịch dùng một lần, ví dụ “Luôn luôn loại bỏ các sản phẩm bị nhiễm máu theo cách phù hợp với các quy trình rủi ro sinh học đã được thiết lập”.
Phụ lục A
(quy định)
Thử nghiệm vật lý
+ Yêu cầu chung
Tất cả các thử nghiệm vật lý phải được thực hiện ở nhiệt độ (23 ± 2) °C trừ khi các nhiệt độ khác được đưa ra trong phương pháp thử nghiệm.
+ Thử nghiệm nhiễm hạt
Nguyên lý:
Các thể hạt được xúc rửa khỏi các bề mặt dẫn dịch bên trong của bộ truyền dịch và thiết bị dẫn khí độc lập, rồi tập hợp trên một màng lọc và đếm trên kính hiển vi.
+ Các chất thử và vật liệu
Nước cất đã lọc qua một màng lọc có kích cỡ lỗ 0,2 μm hoặc chất lượng nước tương đương.
Găng tay không thấm bột.
Bộ lọc hút, màng lọc đơn có kích cỡ lỗ 0,45 μm.
+ Quy trình
Đơn vị lọc, bộ lọc và tất cả các thiết bị khác phải được làm sạch một cách cẩn thận bằng nước cất trước khi thử nghiệm (A.2.2.1).
Xả 10 bộ thiết bị chuẩn bị sử dụng bởi 500 ml nước cất theo A.2.2.1 trong điều kiện dòng chảy phân lớp (trạm làm việc không khí sạch cấp N5 theo TCVN 8664-1 (ISO 14644-1)). Sau đó toàn bộ thể tích nước được lọc hút theo A.2.2.3. Đặt các thể hạt lên trên màng lọc có màn hình ở đô phóng đại 50 lần bằng cách sử dụng kỹ thuật chiêu sáng chéo, rồi đo và đếm theo các hạng kích cỡ đã nêu trong Bảng A.1.
+ Xác định kết quả
Quy định chung:
Thử nghiệm một số lượng thích hợp các bộ truyền dịch đơn (tối thiểu 10 bộ), số lượng thể hạt /10 bộ truyền dịch ở mỗi hạng kích cỡ trong số ba hạng kích cỡ là kết quả thử nghiệm.
Đếm số thể hạt:
Các giá trị thu được từ một mẫu đối chứng rỗng phải được ghi lại trong một báo cáo thử nghiệm và được tính đến khi tính toán giới hạn chỉ số nhiễm.
Mẫu đối chứng trắng là số lượng và kích cỡ thể hạt thu được từ 10 mẫu 500 ml nước tương đương đã phân loại theo 3 hạng kích cỡ trong Bảng A.1, sử dụng cùng một dụng cụ thử nghiệm nhưng không cho qua bộ truyền dịch thử nghiệm.
Số lượng thể hạt trong mẫu rỗng, N0 không được vượt quá giá trị 9. Mặt khác, dụng cụ thử nghiệm phải được tháo ra, làm sạch lại, và lại thực hiện thử nghiệm nền. Các giá trị xác định mẫu rỗng cần được ghi lại trong báo cáo thử nghiệm.
Bảng A.1 - Đánh giá sự nhiễm hạt
Thông số hạt | Hạng kích cỡ | ||
| 1 | 2 | 3 |
Kích cỡ hạt (μm) | 25 đến 50 | 51 đến 100 | > 100 |
Số lượng hạt/10 bộ truyền dịch | na1 | na2 | na3 |
Số lượng hạt trong mẫu đối chứng rỗng | nc1 | nc2 | nc3 |
Hệ số đánh giá | 0,1 | 0,2 | 5 |
Giới hạn chỉ số nhiễm được tính toán như sau:
Đối với mỗi hạng trong số ba hạng kích cỡ, nhân số lượng hạt trong 10 bộ truyền dịch với hệ số đánh giá, và cộng các kết quả để thu được số lượng hạt trong bộ truyền dịch (các mảnh thử nghiệm), Na. Sau đó với mỗi hạng kích cỡ, nhân số lượng hạt trong mẫu đối chứng rỗng với hệ số đánh giá và cộng các kết quả để thu được số lượng hạt trong mẫu trống, Nb.
Lấy Na trừ đi Nb để thu được giới hạn chỉ số nhiễm.
Số lượng hạt trong các bộ truyền dịch (mảnh thử nghiệm):
Na = na1 × 0,1 + na2 × 0,2 + na3 × 5 | (A.1) |
Số lượng hạt trong mẫu đối chứng rỗng:
Nb = nb1 × 0,1 + nb2 × 0,2 + nb3 × 5 | (A.2) |
Giới hạn chỉ số nhiễm:
N = Na - Nb ≤ 90 | (A.3) |
+ Thử nghiệm rò rỉ
Khi bắt đầu thử nghiệm, toàn bộ hệ thống phải được ủ ở nhiệt độ thử nghiệm.
Kết nối bộ truyền dịch với nguồn cung cấp không khí và đóng tất cả các lỗ còn lại. Đặt không khí có áp suất dương bên trong là 50 kPa vào bộ truyền dịch trong 15 s. Áp suất khí quyển phải là áp suất chuẩn. Kiểm tra bộ truyền dịch xem có rò rỉ không khí dưới nước ở (40 ± 1) °C hay không.
Cho đầy nước cất không chứa khí vào bộ truyền dịch. Nối bộ truyền dịch với thiết bị hút và đóng tất cả các lỗ còn lại. Đặt chân không với áp suất âm bên trong 20 kPa trong 15 s. Áp suất khí quyển phải là áp suất chuẩn. Kiểm tra xem không khí có vào bộ truyền dịch hay không.
+ Thử nghiệm độ bền kéo căng
Đặt bộ truyền dịch cần thử nghiệm vào một lực kéo tĩnh 15 N áp dọc theo trục dài trong vòng 15 s. Kiểm tra trực quan bằng mắt xem bộ truyền dịch có chịu được lực kéo hay không.
+ Xác định lưu lượng
Bộ truyền dịch không có thiết bị dẫn khí
Dùng chai hoặc túi chứa đầy tối thiểu 1000 ml dung dịch natri clorua [nồng độ NaCI = 9 g /1]. Nếu sử dụng chai cứng hoặc chai bán cứng cứng thì chai phải được cắt mở ở phía trên để tạo hệ thống thông hơi tự do. Đưa thiết bị đâm xuyên của bộ truyền dịch vào chai hoặc cửa túi. Đổ đầy 2/3 buồng nhỏ giọt. Mở điều tiết lưu lượng và làm đầy bộ truyền dịch. Đóng bộ điều tiết lưu lượng. Bố trí thiết bị thử nghiệm sao cho có độ cao (1 000 ± 5) mm giữa mực chất lỏng của buồng nhỏ giọt và đầu ra của bộ truyền dịch khi bắt đầu thử nghiệm. Mức chất lỏng giữa mực nước trong buồng nhỏ giọt và chai hoặc túi không được vượt quá 300 mm (xem Hình A.1).
Kích thước tính bằng milimét
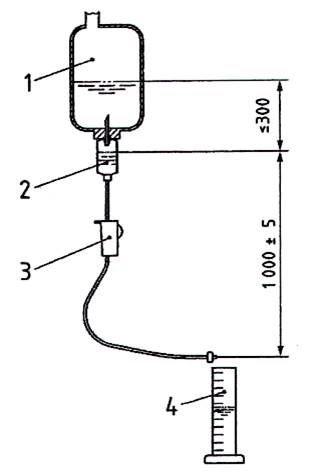
CHÚ DẪN:
1) Chai hoặc túi
2) Thiết bị đâm xuyên
3) Bộ điều tiết lưu lượng
4) Buồng nhỏ giọt
Hình A.1 - Thiết lập thử nghiệm mẫu để xác định lưu lượng
+ Bộ truyền dịch với thiết bị dẫn khí tích hợp
Đóng cửa vào không khí của thiết bị dẫn khí tích hợp của bộ truyền dịch.Thực hiện theo hướng dẫn của A.5.1 đối với bộ truyền dịch và tính tốc độ dòng chảy Q0 = thể tích / lần.
Sử dụng chai chứa cứng. Thực hiện theo hướng dẫn của A.5.1 nhưng không cắt lỗ trong chai. Chai không được thông hơi tự do. Đảm bảo rằng việc đóng thiết bị dẫn khí tích hợp ở vị trí mở. Tính lưu lượng Q1 = thể tích / lần. Lưu lượng Q1 phải đáp ứng yêu cầu
Q1 ≥ Q0 × 0,8 | (A.4) |
+ Bộ truyền dịch với thiết bị dẫn khí độc lập
Thực hiện theo hướng dẫn của A.5.1 đối với bộ truyền dịch mà không sử dụng thiết bị dẫn khí độc lập và tính lưu lượng Q0 = thể tích / lần.
Sử dụng chai chứa cứng. Thực hiện theo hướng dẫn của A.5.1 nhưng không cắt lỗ trong chai. Chai không được thông hơi tự do. Lắp thiết bị dẫn khí độc lập vào sau khi lắp thiết bị đâm xuyên qua nắp của bộ dịch truyền vào chai. Tỉnh lưu lượng Q1 = thể tích / lần. Lưu lượng Q1 phải đáp ứng yêu cầu được đưa ra trong công thức (A.4).
+ Thử nghiệm hiệu suất của bộ lọc dịch
Chuẩn bị dịch thử nghiệm:
Để làm dịch thử nghiệm, sử dụng dịch treo chứa các hạt cao su trong nước với đường kính (20 ± 1) μm và nồng độ xấp xỉ 1000 hạt/100 ml.
Quy trình:
Lắp bộ lọc dịch và đặt nó làm sao để nó tương đương với vị trí sử dụng thực tế trong một dụng cụ thử nghiệm thích hợp theo Hình A.2. cắt đường ống của bộ truyền dịch ở khoảng cách khoảng 100 mm dưới bộ lọc dịch.
Súc bộ lọc dịch bằng 5 ml dịch thử nghiệm từ chai chứa và loại bỏ sản phẩm lọc. Cho 100 ml dịch thử nghiệm chảy qua bộ lọc dịch và tập hợp dịch chảy ra dưới tác dụng hút chân không sau khi đi qua một màng lọc khung lưới màu đen với kích cỡ lỗ (5 - 8) μm và đường kính 47 mm. Đặt màng lọc cùng với các hạt cao su bị giữ lại lên trong một phiến kính kính hiển vi thích hợp và đếm số hạt cao su ở tối thiểu 50 % ô vuông lưới dưới độ phóng đại 50 lần đến 100 lần. Bỏ qua các hạt rõ ràng không phải là cao su.
Tất cả thao tác liên quan trong thử nghiệm này nên được tiến hành trong một môi trường sạch, nếu có thể trong môi trường thông khí thành lớp.
Thể hiện kết quả:
Tỷ lệ giữ hạt của bộ lọc, R, thể hiện bằng tỷ lệ phần trăm như sau:
R = (1 - n1/n0) × 100 | (A.5) |
Trong đó:
n1 là số lượng hạt giữ lại trên màng lọc;
n0 là số lượng hạt trong dịch thử nghiệm đã sử dụng.
Kích thước tính bằng milimét
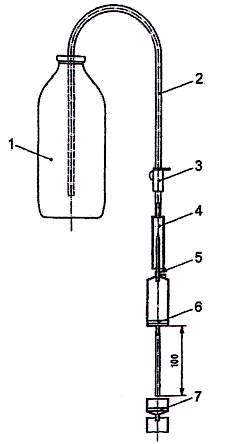
CHÚ DẪN:
1) Chai chứa 2) Ống chuyển dịch 3) Điều tiết lưu lượng 4) Mảnh kết nối | 5) Thiết bị xuyên nắp 6) Bộ lọc dịch 7) Màng lọc |
Hình A.2 - Thiết lập dụng cụ mẫu để thử nghiệm hiệu quả của bộ lọc dịch
+ Thử nghiệm vị trí bơm thuốc
Đặt vị trí bơm thuốc nằm ngang ở tư thế không bị đè. Cho đày nước vào bộ truyền dịch làm sao để không xuất hiện bọt khí giữ lại trong bộ truyền và áp một áp suất 20 kPa trên áp xuất khí quyển. Đâm thủng vị trí bơm thuốc tại vùng đã đánh dấu trước bằng một kim tiêm dưới da có đường kính ngoài 0,8 mm và phù hợp với ISO 7864. Để nguyên kim trong vòng 15 s. Lấy kim ra và ngay sau đó thấm khô vị trí đâm xuyên. Sau thời gian 1 min, quan sát xem có dấu hiệu rò dịch từ vị trí tiêm hay không. Trong trường hợp thiết kế vị trí tiêm khác, nên thực hiện thử nghiệm bằng cách tiêm vào vị trí đó theo hướng dẫn do nhà sản xuất cung cấp.
Phụ lục B
(quy định)
Thử nghiệm hóa học
+ Chuẩn bị dịch chiết S1 và dịch rỗng S0
Dịch chiết S1:
Tạo một hệ thống tuần hoàn kín gồm ba bộ truyền dịch và một bình cầu cổ dài bằng thủy tinh borosilicat 300 ml. Lắp vào bình cầu một thiết bị điều chỉnh nhiệt duy trì nhiệt độ trong dung dịch bình cầu ở nhiệt độ (37±1) °C. Cho tuần hoàn 250 ml nước, phù hợp với cấp độ 1 và 2 của TCVN 4851 (ISO 3696), qua hệ thống trong vòng 2 h với lưu lượng 1 l/h, chẳng hạn bằng cách sử dụng một bơm nhu động gắn vào một ống Silicon thích hợp càng ngắn càng tốt. Tập hợp tất cả dịch và để nguội.
Dịch rỗng S0:
Dịch rỗng S0 được chuẩn bị giống như mô tả đối với dịch S1 nhưng bỏ các bộ truyền dịch ra khỏi hệ tuần hoàn. Dung dịch chiết S1 và dung dịch rỗng S0 phải được sử dụng cho các thử nghiệm hóa học.
+ Các thử nghiệm tìm chất khử (có thể bị oxy hóa)
Thêm 10 ml dung dịch S1 vào 10 ml dung dịch KMnO4 nồng độ c(KmnO4) = 0,002 mol/l và 1 ml dung dịch H2SO4 nồng độ 1 mol/l, lắc và để cho chúng phản ứng trong vòng 15 min ở nhiệt độ (23 ± 2) °C.
Sau khi thêm 0,1 g KI (kali iot), chuẩn độ dung dịch theo một dung dịch thể tích chuẩn natri thiosulphat với nồng độ c(Na2S2O3) = 0,005 mol/l, cho đến khi nó trở thành màu nâu sáng. Thêm 5 giọt dung dịch tinh bột và tiếp tục chuẩn độ cho đến khi màu xanh biến mất.
Tiến hành một thử nghiệm rỗng đồng thời.
Tính toán hiệu, theo ml, thể tích của dung dịch Na2S2O3 0,005 mol/l làm dung dịch chiết S1 và thể tích dung dịch Na2S2O3 làm dung dịch rỗng S0.
+ Thử nghiệm tìm ion kim loại
Thử nghiệm 10 ml dung dịch chiết S1 tìm ion kim loại, sử dụng các quy trình đã được chấp nhận bởi các dược điển quốc gia. Xác định mức độ hiện màu.
+ Thử nghiệm chuẩn độ axit hoặc kiềm
Thêm 0,1 ml dung dịch chỉ thị Tashiro vào 20 ml dung dịch chiết S1 trong một bình cầu chuẩn độ.
Nếu màu của dung dịch tạo thành là tím, chuẩn độ với dung dịch thể tích chuẩn Na(OH) nồng độ 0,01 mol/l, và nếu màu xanh, chuẩn độ với dung dịch thể tích chuẩn HCI nồng độ 0,01 mol./l cho đến khi xuất hiện màu xám nhạt.
Thể hiện thể tích dung dịch Na(OH) hay HCl đã sử dụng theo mililit (mm).
+ Thử nghiệm tìm chất tồn dư không bay hơi
Chuyển 50 ml dung dịch chiết S1 vào một đĩa tự bay hơi, và để bay hơi đến độ khô ở nhiệt độ ngay dưới nhiệt độ sôi. Làm khô đến khối lượng không đổi ở 105 °C.
Xử lý 50 ml dung dịch rỗng S0 theo cách tương tự.
Thể hiện hiệu giữa các khối lượng tồn dư thu được từ dung dịch chiết S1 và dung dịch rỗng S0 theo mg.
+ Thử nghiệm sự hấp thu
Cho dung dịch chiết S1 qua một màng lọc có kích cỡ lỗ 0,45 μm để tránh các giao thoa tán ánh sáng lạc. Trong vòng 5 h chuẩn bị, đặt dung dịch vào một thiết bị đo quét quang phổ UV ở một buồng thạch anh 1cm cùng với dung dịch rỗng S0 trong một buồng tham chiếu và ghi lại quang phổ trong bước sóng từ 250 nm đến 320 nm.
Báo cáo kết quả dưới dạng biểu đồ ghi, thể hiện đường hấp thu theo bước sóng.
Phụ lục C
(quy định)
Thử nghiệm sinh học
+ Thử nghiệm tính gây sốt
Thử nghiệm tính gây sốt cần được thực hiện như đã mô tả trong các dược điển quốc gia hay các tiêu chuẩn quốc gia.
CHÚ THÍCH: Một thử nghiệm tìm các chất gây sốt và nội độc tố vi khuẩn được mô tả trong Dược điển Châu Âu và trong Dược điển Mỹ.
+ Thử nghiệm để đánh giá sinh học
Các phương pháp thử nghiệm dùng để đánh giá sinh học như đã mô tả trong TCVN 7391-1 (ISO 10993-1) nên được coi là chi dẫn khi đánh giá tính tương thích sinh học.
Thư mục tài liệu tham khảo
[1] TCVN 9848:2013 (ISO 291:2008), Chất dẻo - Khí quyển tiêu chuẩn cho ổn định và thử nghiệm.
[2] ISO 7000, Graphical symbols for use on equiμment -Registered symbols (Các ký hiệu đồ họa để sử dụng trên thiết bị - Các ký hiệu đã đăng ký).
[3] TCVN 7391-1:2004 (ISO 10993-1:2003), Đánh giá sinh học trang thiết bị y tế - Phần 1: Đánh giá và thử nghiệm.
[4] TCVN 7391 -4:2005 (ISO 10993-4:2002), Đánh giá sinh học trang thiết bị y tế - Phần 4: Chọn phép thử tương tác với máu.
[5] TCVN 7392 (ISO 11135), Tiệt khuẩn sản phẩm chăm sóc sức khỏe - Ethylen oxit.
[6] TCVN 7393-1 (ISO t1137-1), Tiệt khuẩn sản phẩm chăm sóc sức khỏe - Bức xạ - Phần 1: Yêu cầu triển khai, đánh giá xác nhận và kiểm soát thường quy quá trình tiệt khuẩn đối với thiết bị y tế.
[7] TCVN 7393-2 (ISO 11137-2), Tiệt khuẩn sản phẩm chăm sóc sức khỏe - Bức xạ - Phần 2: Thiết lập liều tiệt khuẩn.
[8] TCVN 7394-1 (ISO 11607-1), Bao gói trang thiết bị y tế đã tiệt khuẩn - Phần 1: Yêu cầu đối với vật liệu, hệ thống bảo vệ vô khuẩn và hệ thống bao gói.
[9] TCVN 7394-2 (ISO 11607-2), Bao gói trang thiết bị y tế đã tiệt khuẩn - Phần 2: Yêu cầu đánh giá xác nhận đối với quá trình tạo hình, niêm kín và lắp ráp.
[10] ISO 17665-1, Sterilization of health care products - Moist heat - Part 1: Requirements for the development, validation and routine control of a sterilization process for medical devices (Tiệt khuẩn các sản phẩm chăm sóc sức khỏe - Nhiệt ẩm - Phần 1: Yêu cầu đối với việc phát triển, xác nhận và kiểm soát thường quy quy trình tiệt trùng cho các thiết bị y tế)
[11] ISO/TS 17665-2, Sterilization of health care products - Moist heat - Part 2: Guidance on the application of ISO 17665-1 (Tiệt khuẩn các sản phẩm chăm sóc sức khỏe - Nhiệt ẩm - Phần 2: Hướng dẫn áp dụng ISO 17665-1)
[12] ISO 80369-20:2015, Small-bore connectors for liquids and gases in healthcare applications - Part 20: Common test methods (Đầu nối nòng nhỏ cho chất lỏng và khí trong các ứng dụng chăm sóc sức khỏe - Phần 20: Các phương pháp thử nghiệm thông thường)
[13] European Pharmacopoeia (Dược điển Châu Âu) (xem http://www.edqm.eu)
[14] United stated Pharmacopoeia (Dược điển Mỹ) (xem http: //www.usp.org)
[15] Japanese Pharmacopoeia (Dược điển Nhật Bản) (xem https://www.pmda.go.jp)










